はじめに
化学というと難しそうに聞こえますが、実は身近な現象や実験を通じて理解することができます。その一つが「滴定曲線」です。今回は、化学の基礎である滴定曲線について、分かりやすく説明していきます!
滴定曲線
滴定とは
滴定とは、ある物質の濃度を調べるために、別の物質を少しずつ加えて反応させ、その変化を観察する方法です。例えば、レモンジュースの酸の濃さを調べるときに、塩基(アルカリ性の物質)を少しずつ加えていき、その変化を見ます。
pH指示薬
滴定を行う際に、反応の進行を目で見て確認するために使われるのが「pH指示薬」です。pH指示薬は、溶液のpHによって色が変わる物質です。これにより、酸や塩基がどのくらいの量で中和されるかを簡単に判断することができます。
pH指示薬には様々な種類がありますが、ここではメチルオレンジとフェノールフタレインについて説明します。
メチルオレンジ
メチルオレンジは、酸性から中性付近で色が変わるpH指示薬です。
- 酸性(pH 3.1以下):赤色
- 中性から塩基性(pH 4.4以上)黄色
中和点付近で色が赤→黄色に変わる!
フェノールフタレイン
フェノールフタレインは、弱酸性から塩基性で色が変わるpH指示薬です。
- 酸性から中性(pH 8.2以下):無色
- 塩基性(pH 10.0以上):赤色(ピンク色)
中和点付近で無色→赤紫色に変わる!
強酸・強塩基の滴定曲線
強酸に強塩基を滴下する!(コニカルビーカに強酸、ビュレットに強塩基)


pHが急に上昇する(pHジャンプとも言う)ところの中心が中和点🟢(pH7)になる!

適切なpH指示薬の選び方!
pHが急に上昇する(pHジャンプとも言う)ところにpH指示薬の変色域が被っていれば、適切な指示薬と言える!
※塩基に酸を滴定する場合は、pHが急に下降するところ
強酸・強塩基の滴定の場合、適切なpH指示薬はフェノールフタレインとメチルオレンジである!
強塩基に強酸を滴下する!(コニカルビーカに強塩基、ビュレットに強酸)
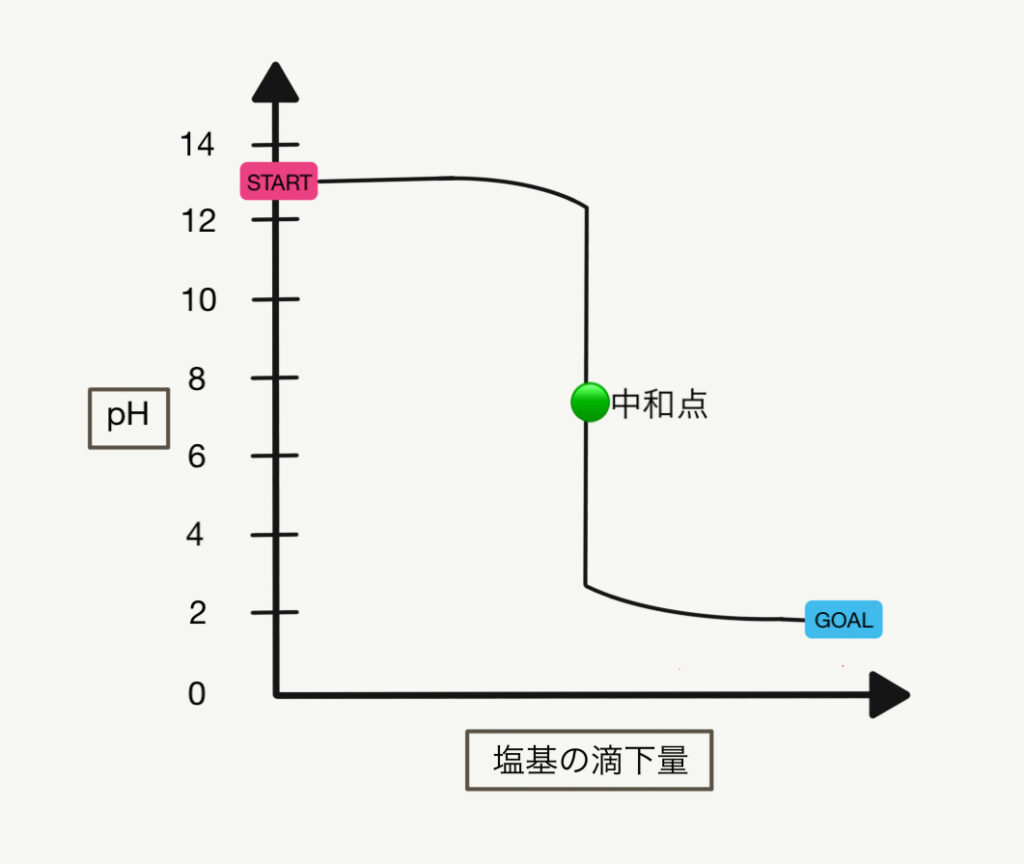
弱酸・強塩基の滴定曲線
弱酸に強塩基を滴下する!
手順は、強酸・強塩基のときと同じ!(省略)
弱酸・強塩基の滴定の場合は、フェノールフタレインを用いる!
強塩基に弱酸を滴下する

強酸・弱塩基の滴定曲線
強酸に弱塩基を滴下する
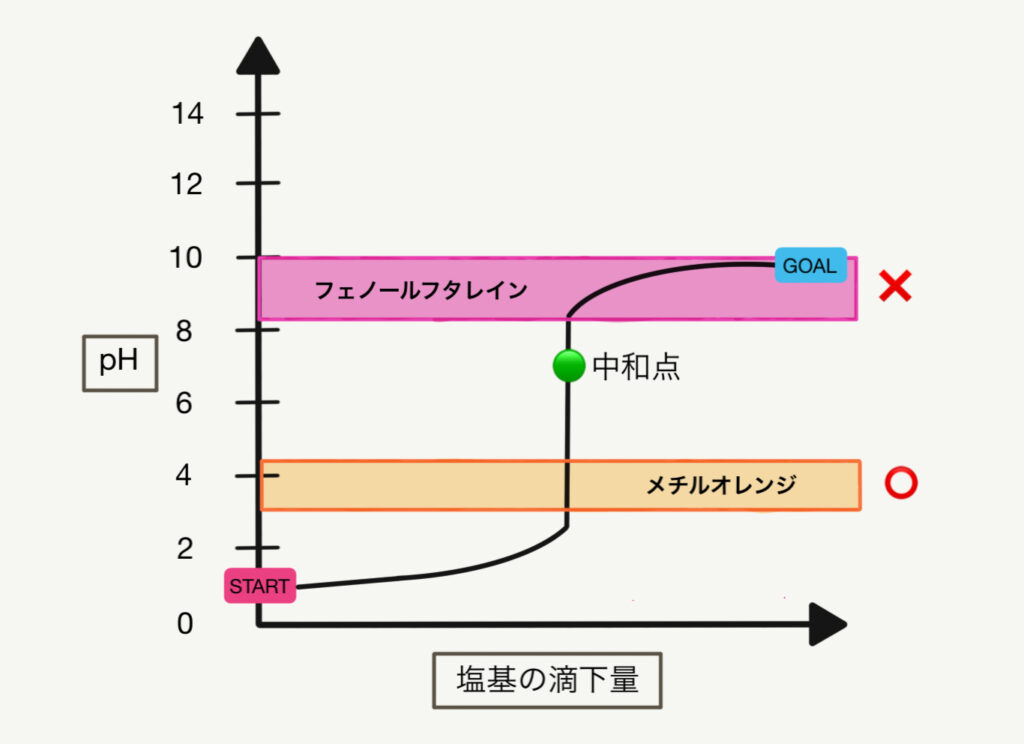
強酸・弱塩基の滴定の場合は、メチルオレンジを用いる!
弱塩基に強酸を滴下する

弱酸・弱塩基の滴定曲線
弱酸に弱塩基を滴下

弱塩基に弱酸を滴下

弱酸・弱塩基の場合は適切なpH指示薬がない!
まとめ
①強酸・強塩基→フェノールフタレイン,メチルオレンジ
②弱酸・強塩基→ フェノールフタレイン
③強酸・弱塩基→ メチルオレンジ
④弱酸・弱塩基→ どちらも不適
なぜ滴定曲線が重要なのか?
滴定曲線を使うことで、以下のようなことが分かります:
- 物質の濃度の正確な測定:中和点を知ることで、酸や塩基の正確な濃度を求めることができます。
- 化学反応の理解:酸と塩基がどのように反応するのか、その過程を視覚的に理解することができます。
例えば、食品の酸性度を測定することで、安全性や品質管理に役立てることができます。
日常生活への応用
滴定曲線は化学の実験だけでなく、日常生活にも応用できます。
- 食品の品質管理:レモンジュースやワインの酸性度を測定して品質を保つ。
- 環境調査:水質調査で湖や川の酸性度を測定して環境保護に役立てる。
さいごに
滴定曲線は、化学の基礎を理解するための重要なツールです。最初は難しく感じるかもしれませんが、実験を通じてその仕組みを理解することで、より身近なものに感じられるでしょう。滴定曲線を学ぶことで、物質の性質や反応を深く理解することができ、日常生活にも役立つ知識を身につけることができます!
これからも文系の方にもわかるように、化学基礎・化学を解説していきますのでチェックお願いします!






コメント