はじめに
こんにちは、皆さん!今回は、「電気分解」についてわかりやすく解説していきます。電気分解は、高校化学の範囲で学ぶ重要な概念の一つですが、文系の方にも理解しやすいように噛み砕いて説明します。
電気分解とは?
電解質の水溶液に電極を浸し、電流を流したとき電極の表面で起こる酸化還元反応。
陽極:電源の正極につないだ電極
陰極:電源の負極につないだ電極
陰極・陽極で反応する順番を覚えておこう!
陰極で反応する順番
①Ag+,Cu2+などのイオン化傾向が小さい金属のイオン!
②H+
③H2O
④SO42−,NO3−などの多原子イオン!
陽極で反応する順番
①極板がAg,Cuのどちらかのとき
②ハロゲンのイオン(Cl−,Br−など)
③OH−
④SO42−,NO3−などの多原子イオン!
塩化銅CuCl2水溶液の電気分解についてみてみよう!
塩化銅水溶液の電気分解では、正極、負極ともに炭素の極板を使い塩化銅CuCl2水溶液を電気分解する!
イラストでイメージしよう!

化学反応式を書いてみよう!
陰極での反応
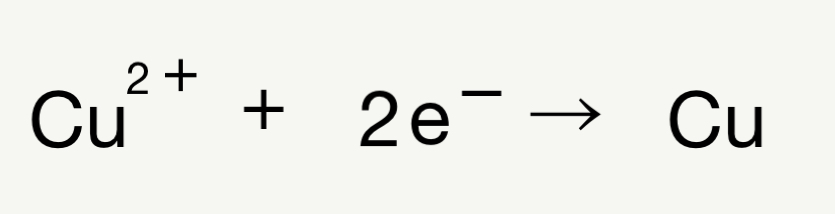
- 溶液中の銅イオンと負極から送られてきた、電子2つが反応する!
- ①より銅が生成され、陰極の極板に張り付く形で析出する!
- 銅イオンは電子を受け取ったため、還元された!
陽極での反応

- 溶液中の塩化物イオンは電子を陽極に渡す!
- 塩化物イオンは電子を失ったため、塩素となり陽極側に気体となって発生する!
- 塩化物イオンは電子を失ったため、酸化した!
応用と実用例
電気分解は、様々な産業で重要な役割を果たしています。
- アルミニウムの精錬:
-
ボーキサイト鉱石からアルミニウムを抽出するために電気分解が使われます。
- 水の電気分解による水素製造:
-
クリーンエネルギーとして注目される水素ガスの生成に使われます。
電気分解の利点
まとめ
電気分解は、化学反応を電気の力で進める技術です。基本的な仕組みを理解することで、その応用範囲の広さに驚かされます。日常生活から産業まで、電気分解は私たちの生活を支える重要な技術です。
問題なども、随時作っていきますのでお楽しみください!この記事を見ながら、たくさんの問題に取り組みましょう!以下におすすめの教材を貼っておきます!
これからも文系の方にもわかるように、化学基礎・化学を解説していきますのでチェックお願いします!

化学基礎 電池の仕組み 5分でわかる! – 科学の部屋
目次 はじめに電池の仕組みボルタ電池おわりに はじめに 今回は電池の仕組みについて簡単に解説します。日常生活で欠かせない電池ですが、その仕組み…
科学の部屋

化学基礎 ダニエル電池 5分でわかる! – 科学の部屋
目次 はじめにダニエル電池って何?ダニエル電池の基本的な仕組みダニエル電池の構造と化学反応式おわりに はじめに 化学に興味がある文系の皆さんに…
科学の部屋

化学基礎 鉛蓄電池 5分でわかる! – 科学の部屋
目次 はじめに鉛蓄電池とは鉛蓄電池の歴史鉛蓄電池の仕組み鉛蓄電池の利点と欠点豆知識と逸話おわりに はじめに こんにちは、皆さん!今回は、私たち…
科学の部屋









コメント