はじめに(覚え方も!)
・同素体とは、同じ元素でも構造と性質が異なる物質のこと。
・炭素、酸素、硫黄、リン(この4つだけ!)などの元素は、それぞれ複数の同素体を持ちます。ここでは、各元素の同素体の特性をリストアップして解説します!
※まとめだけでも最低限覚えよう!
覚え方!
スコップ(SCOP)で同素体を掘り当てよう!
炭素(C)
黒鉛(Graphite)
見た目:灰色の固体で、黒っぽい色合いを持つ。
用途:鉛筆の芯や半導体に使用される。
性質:電気・熱をよく通す。また潤滑性(滑りやすい)がある

基本的な構造:
グラフェンは図のように、正六角形の構造をとっている。

立体的な構造:
①正六角形が繰り返され、シート上の平面構造になっている。
②シートが上下方向に、何枚も重なっている。
③1つの炭素(赤い🔴に注目!)に注目すると他の3つの炭素と結合している。

鉛筆で文字が書ける理由
①シートの間はとても弱い結合(分子間力)でくっついている!
②力を少しかけると、①の結合が壊れ紙に炭素の粒子が付着する!
ダイヤモンド(diamond)
見た目:無色透明
用途:
① 宝石(指輪など)
② 精密機器や切削工具(産業の製品)
③ 投資(投資の対象としても扱われる)
性質:
① 硬度 (地球上で最も硬い物質の1つ)
② 輝き (光を反射して美しい輝きを放つ)
③ 透明性 (通常は透明で、内部から光を反射する)
④ 電気・熱を通さない

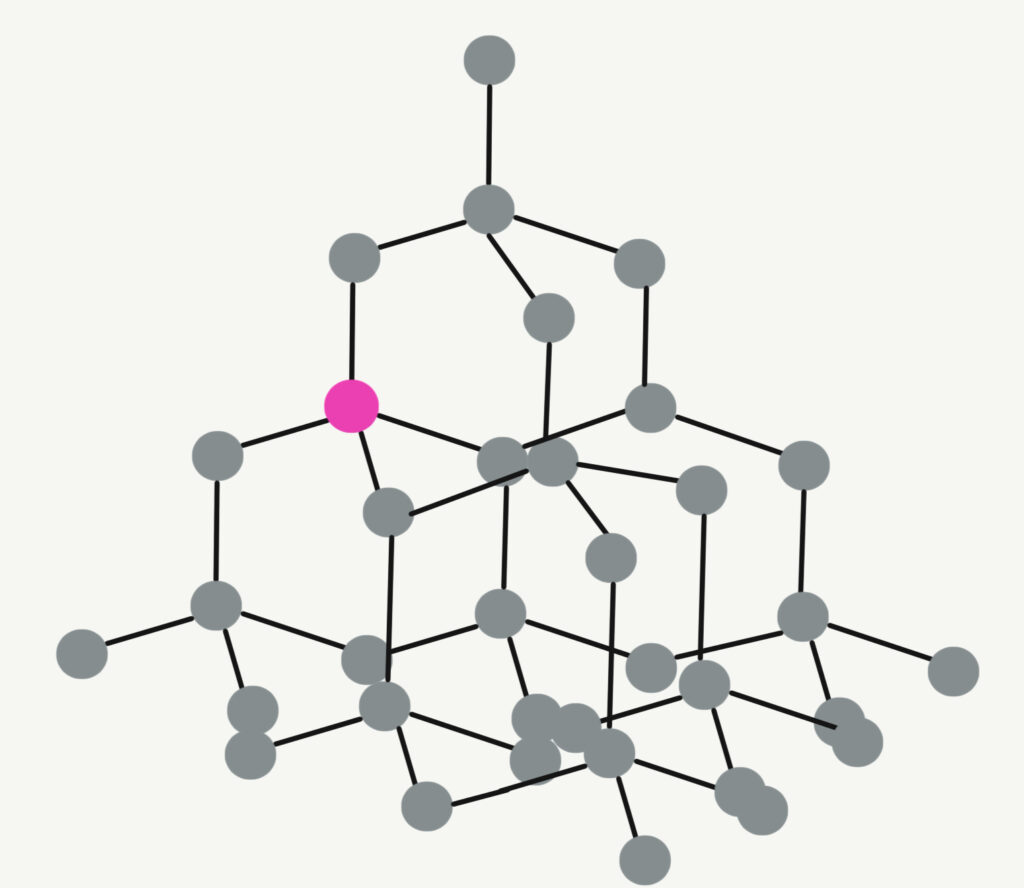
基本的な構造:
ダイヤモンドは図のように正四面体(ピラミッドの形)の構造をとっている。

立体的な構造:
① 正四面体が繰り返された立体構造になって
いる。
② 1つの炭素(赤い🔴に注目!)に注目すると他の4つの炭素と結合している。
③ 全てが強い結合!→なので超硬い!
フラーレン(Fullerene)
見た目:球形(サッカーボールのような構造)
用途:
① 医学(がん治療や画像診断など)
② 材料工学(高性能な材料の開発)
性質:
① 強度(ダイヤモンド並の硬さ)
② 電気・熱をよく通す

黒鉛とダイヤモンドの違い(まとめ)

発展!電気を通す?通さない?
①黒鉛は、1つの粒子に注目す ると、3つの炭素と結合している!(炭素は4つまで結合できる!)
②①より結合の手が1つ余っている!(結合の手=電子)
③②より黒鉛は電気を通す!(ダイヤモンドは電子が余っていないため、通さない)
酸素(O)
酸素(oxygen)
見た目:気体(無色透明、無臭)
性質・特徴:
①酸化作用 ②燃焼(酸素がないと物が燃えない) ③空気中に約21%ほど含まれる。
オゾンO3(Ozone)
見た目:気体(淡い青色、刺激臭)
性質・特徴:
①オゾン層
地球の上空に存在し、紫外線を吸収して地表に届く量を減らし、地球を保護している。
②酸化力
強力な酸化作用を持ち、雑菌やウイルスを除去する消毒効果がある。

リンP(phosphorus)
黄リン
見た目:淡い黄色い固体
性質・特徴:①猛毒、②自然発火(水中で保存する)
構造式:S4(不安定な構造)

赤リン
見た目:赤褐色の粉末
性質・特徴:
①マッチの側面や、神社の鳥居の色に使われている。
②毒性は低い
構造式:Sx(安定な構造)

硫黄(sulfur)
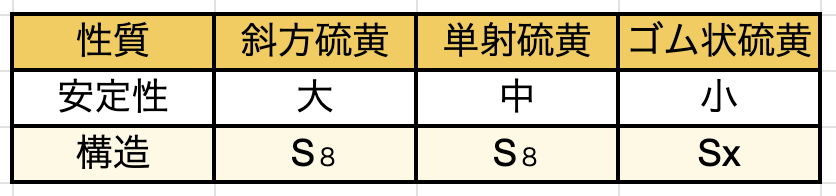
斜方硫黄
見た目:大きいな黄色の結晶
性質・特徴:常温で安定、火薬の原料や医薬品に使われる。
構造式:S8

単斜硫黄
見た目:黄色い針状の結晶。常温で放置すると斜方硫黄になる
性質・特徴:常温で放置すると斜方硫黄になる
構造式:S8

ゴム状硫黄
見た目:ゴムに似た弾性をもち、褐色〜黄色になる
性質・特徴:ゴムのように伸び、非常に不安定
構造式:Sx

硫黄(まとめ)
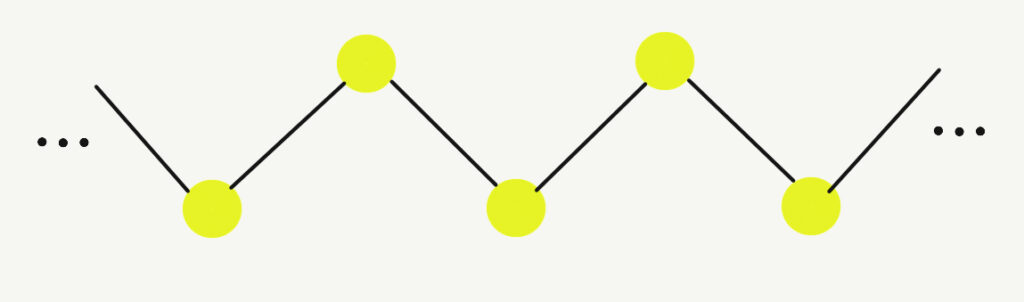
・構造式について(おまけ)
・S8:図のように王冠のような構造をしている

・Sx:図のような構造が左右にtくさん続いている。そのため、ゴムのような性質になる
まとめ
・同素体:同じ元素でできているもの(構造が違えば、性質も違う)
・覚え方:SCOP(スコップ)
・炭素:黒鉛、ダイヤモンド、フラーレン(ダイヤモンドと、黒鉛の違いも抑えよう!)
・酸素:酸素、オゾン
・リン:黄リン、赤リン
・硫黄:斜方硫黄、単斜硫黄、ゴム状硫黄(安定性抑えよう!)
※ 以下は化学に関する教材の宣伝・広告です。








コメント